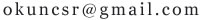一道化学计算题,求详细过程!速度!!!
某化学兴趣小组的同学为测定石灰石样品中碳酸钙的含量(杂质不溶于水也不溶于酸),同学们取石灰石样品16克,放入68.4克盐酸中,测得物质总质量的变化如图所示,求:
(1)原混合物中碳酸钙的含量;
(2)反应后所得溶液中溶质的质量分数.

含杂质物质的化学反应的有关计算;有关溶质质量分数的简单计算;碳酸钠、碳酸氢钠与碳酸钙;盐的化学性质;根据化学反应方程式的计算.
【专题】
溶质质量分数与化学方程式相结合的计算.
【分析】
(1)因为碳酸钙和盐酸反应后会产生二氧化碳气体,所以烧杯中物质总质量会减少,根据质量守恒定律可知,烧杯中物质总质量的减少量就是生成的二氧化碳的质量,根据化学方程式利用二氧化碳的质量可得到碳酸钙的质量;
(2)根据碳酸钙和盐酸反应的化学方程式,利用二氧化碳的质量可求出生成的氯化钙的质量,进而求出氯化钙的质量分数,其中反应后溶液的质量=参加反应的固体质量+液体质量-生成的沉淀质量-生成的气体质量.
【解答】
解:(1)通过图象可知,反应产生的二氧化碳的质量为:84.4g-80g=4.4g
设原混合物中碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 111 44
x y 4.4g
100/44=x/4.4g
x=10g
(2)设反应产生的CaCl2的质量为y
111/44=y/4.4g
y=11.1g
反应后溶液质量=10g+68.4g-4.4g=74g
所以反应后CaCl2的质量分数为:11.1g/74g×100%=15%
答:(1)原混合物中碳酸钙的含量是10g;(2)反应后所得溶液中溶质的质量分数是15%.
CaCO3 + 2HCl = CaCl2 + CO2↑ + H2O
100g 111 44g
10 11.1 4.4
(1)原混合物中碳酸钙的含量=10/16*100%=62.5%
2.反应后所得溶液中溶质的质量分数=11.1/(80-6)*100%=15%
不懂问
CaCO3+2HCl==CaCl2+H2O+CO2↑
100 111 44
x y 4.4g
100/x=111/y=44/4.4g
x=10g
y=11.1g
(1)原混合物中碳酸钙的含量 10g;
(2)反应后所得溶液中溶质的质量分数 11.1g/(10g+68.4g-4.4g)*100%=15%.
CaCO₃+2HCL==CaCl₂+H₂O+CO₂↑
100 73 111 44
a b c 4.4
解得a=10g, b=7.3g(说明盐酸过量,样品已经充分反应), c=11.1
CaCO₃含量=10/16=62.5%
(2)
杂质含量d=16-10=6g
溶质为CaCl₂,其溶液质量分数=11.1/(80-6)=15%
[溶液质量要减去不溶性杂质6g]
设碳酸钙是x g,氯化钙是y个
2HCI+CaCO3=CaCl2+CO2+H2O
100 111 44
x g y g 4.4g
x=10.0g
y=11.1g
碳酸钙是10.0g,
氯化钙的质量分数:11.1/80=13.875%
CaCO3+2H+ =H2O+Ca2+ +CO2气体符合
1 1
x 0.1
n碳酸钙=0.1mol,m碳酸钙=10g
原混合物中碳酸钙的含量为10/16=0.625
生成氯化钙0.1mol,即11.1g
溶质的质量分数11.1/80=0.139
一道化学计算题,求详细过程!速度!!!
(1)因为碳酸钙和盐酸反应后会产生二氧化碳气体,所以烧杯中物质总质量会减少,根据质量守恒定律可知,烧杯中物质总质量的减少量就是生成的二氧化碳的质量,根据化学方程式利用二氧化碳的质量可得到碳酸钙的质量;(2)根据碳酸钙和盐酸反应的化学方程式,利用二氧化碳的质量可求出生成的氯化钙的质量,进而求出...
一道化学计算题!!!速度求求求!!
解:设生成铜x克 Fe+CuSO4=FeSO4+Cu.---Cu-Fe 56---64---8 ---x---56.6-55 64:8=x:(56.6-55)x=12.8 答:生成铜12.8克
一道化学计算题,详见问题补充,详细过程
m(Fe) m(HCl) m(FeCl2) 0.4 解得: m(Fe)= 11.2(g) m(HCl)= 14.6(g) m(FeCl2)=25.4g)1 原混合物中铁粉质量分数= 11.2\/14=80 2 稀释前后溶质的物质的量不变.C1V1=m1\/M=C2V2 14.6\/36.5= 1000*1.19*36%\/36.5 *V2 解得:V = 34.1 (ml...
这一道化学的计算题,求详细步骤。
假设参与反应的氯气的质量是x,生成的碘的质量是y,那么最终得到的固体物质的质量17.5g = (22.5+ x)- y → 变换,得y= (22.5 + x)-17.5 氯气的分子量是71,碘的分子量是254,代入反应方程式:71:x=254:{(22.5 + x)-17.5} 解得:x=1.940(保留3位小数)这种题的关键就...
一道化学计算题,要详细过程!!!
1、减轻的质量为H2的质量100g+15g-114.6g=0.4g n(H2)=0.4g\/2gmol-1=0.2mol V(H2)=0.4\/0.09=4.44L 2、发生的反应为Zn+H2SO4=ZnSO4+H2 n(Zn)=n(H2)=0.2mol m(Zn)=0.2*65=13g 纯度为13\/15*100%=86.7 3、反应后溶质为ZnSO4 m(ZnSO4)=0.2*161=32.2g 质量分数...
初中化学计算题(希望大家写详细点)
Cu的质量=50g*80%*80%+50g*(1-80%)=42g 解析:CuO和H2SO4反应没有固体生成,所以滤渣为CU。根据方程式求CuO的质量,再除以全部的质量,即为氧化铜的质量分数。求出氧化铜中铜的质量分数,把氧化铜中铜的质量和铜单质的质量相加,即为铜的质量。PS:全部是初中化学的格式。偶已经尽最大努力写...
一道化学计算题!!急用!在线等~ 要过程!
1.化学方程式:Mg+H2SO4===H2+MgSO4 依题:有2gMg反应,设有xgMgSO4生成 24x=2*120 所以x=10g 第二个还填18g,依据前面的,5gMg就可以反应完H2SO4了,故还是18g.2.设有yg硫酸.依题意:4g 镁就可以与希硫酸完全反应 24y=98*4 所以y=16 所以硫酸浓度为16\/150*100%=10.7 注:150是由900...
急求!!化学方程式计算题(详细过程)
首先你要知道,氢气是铁与酸反应生成的 (1)Fe+H2SO4===H2+FeSO4 56 2 152 X 0,1 Y X=2.8(g)Y=7.6g (2)所得溶液是硫酸亚铁 根据质量守恒定律,反应前后质量相等,饭杂志不与酸反应,所以反应前m=2.8+25=27.8(g)反应后,氢气走掉了m=27.8-0.1=27.7 FeSO4%=7.6\/27.7=27...
初三化学计算题(要详细过程)
题一:(1)解:设样品中碳酸钠的质量为X Na2CO3+2HCl == 2NaCl+H2O+CO2(向上气体箭头省略)106 44 X 3.52g 列式:106\/44=X\/3.52g 则X=8.48g 碳酸钠的质量分数=8.48g\/10g=84.8 (2)样品中钠元素的质量=8.48g*46\/106+(10g-8.48g)*23\/58.5 =3.68g+0.6g =4.28g ...
一道化学计算题!!! 急用!!!
解:(1)这题可以从氯化钠溶液先入手 ∵溶剂的质量=溶液质量-溶质质量=30kg-30kg*16%=25.2kg 因为溶剂为水,而只有10%的氯化钠溶液中含有水分 ∴可以设10%的氯化钠溶液为Xkg ∴(1-10%)X=25.2 ∴解得:X=28 ∴可得氯化钠固体的质量=30kg-28kg=2kg ∴需要需要氯化钠溶液28kg和氯化钠...